El pasado 7 agosto 2014, se publicó en el BOE la Orden SSI/1478/2014, de 1 de agosto, por la que se incluye la sustancia 4-metilanfetamina en la lista I del anexo I del Real Decreto 2829/1977. Ello quiere decir que desde el día 8 agosto, está prohibido el uso, la fabricación, importación, exportación, tránsito, comercio, distribución y tenencia, así como la inclusión de esta sustancia en todo tipo de preparado.
 Podríamos pensar que es la enésima actualización de este vetusto real decreto, que incluye en sus anexos la trasposición a nuestro ordenamiento jurídico de la conocida como lista verde de sustancias psicotrópicas sometidas a fiscalización internacional, en cumplimiento de la Convención de Sustancias Psicotrópicas de 1971. Lo que pasa es que al leerlo con detenimiento nos encontramos con alguna particularidad relacionada con la 4 –metilanfetamina, a saber:
Podríamos pensar que es la enésima actualización de este vetusto real decreto, que incluye en sus anexos la trasposición a nuestro ordenamiento jurídico de la conocida como lista verde de sustancias psicotrópicas sometidas a fiscalización internacional, en cumplimiento de la Convención de Sustancias Psicotrópicas de 1971. Lo que pasa es que al leerlo con detenimiento nos encontramos con alguna particularidad relacionada con la 4 –metilanfetamina, a saber:
- no se trata de una actualización de nuestra normativa nacional a la citada lista verde de sustancias psicotrópicas sometidas a fiscalización internacional, puesto que estas sustancia no aparece en ella por ningún sitio.
- El origen de la Orden publicada en el BOE procede de la Decisión 2013/129/UE del Consejo, de 7 de marzo de 2013, por la que se somete la 4-metilanfetamina a medidas de control, define la 4-metilanfetamina (en adelante 4-MA) como una nueva sustancia psicotrópica que debe de estar sujeta a medidas de control y a sanciones penales, previstas en la legislación nacional vigente en la materia, de conformidad con las obligaciones contraídas en virtud del Convenio sobre Sustancias Psicotrópicas de 1971 de las Naciones Unidas.
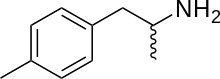 Nótese que el texto legal define a la 4-MA como una nueva sustancia psicotrópica, cuando esta sustancia fue sintetizada en el 1952 como supresora del apetito con el nombre de Aptrol, aunque nunca llegó a comercializarse el fármaco en la Unión Europea. Desde entonces, hay constancia de su utilización como nueva droga de síntesis y como precursor de anfetamina. Últimamente ha sido detectada como componente del speed, relacionándose con graves intoxicaciones y muertes.
Nótese que el texto legal define a la 4-MA como una nueva sustancia psicotrópica, cuando esta sustancia fue sintetizada en el 1952 como supresora del apetito con el nombre de Aptrol, aunque nunca llegó a comercializarse el fármaco en la Unión Europea. Desde entonces, hay constancia de su utilización como nueva droga de síntesis y como precursor de anfetamina. Últimamente ha sido detectada como componente del speed, relacionándose con graves intoxicaciones y muertes.
El sistema de las Naciones Unidas no está evaluando actualmente la 4-MA ni lo ha hecho anteriormente, con el fin de incluirla de algún modo en la lista verde de la mencionada Convención de Sustancias Psicotrópicas de 1971.
La Decisión comunitaria viene motivada porque la 4-MA es un derivado sintético metilado en el anillo de anfetamina que ha sido aprehendido predominantemente en forma de polvo y de pasta en muestras que contenían anfetamina y cafeína, pero que ha aparecido también en pastillas y en forma líquida. Se ha detectado en el mercado ilegal de anfetamina, donde se vende y se consume junto con los fármacos legales aún existentes en algunos países, que contienen anfetamina. Se ha denunciado un caso de detección de esta sustancia en un producto comercial vendido en internet.
El principal precursor químico para la síntesis de la 4-MA es la 4-metilbencil-metil-cetona, que parece estar comercialmente disponible en internet y no está controlada por la normativa internacional que controlan los movimientos de sustancias precursoras de la síntesis de drogas de tráfico ilícito (la conocida como lista roja)[1]. Ello unido a que en estados miembros se estaba restringiendo el control ejercido sobre esta sustancia, ha motivado la decisión comunitaria de prohibir esta sustancia, adoptando un criterio común en toda la Unión Europea.
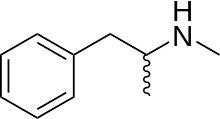 Esto nos lleva a preguntarnos por qué no se actúa de igual forma con la metanfetamina, conocida sustancia psicotrópica que ésta causando estragos con rango de epidemia, generando una adicción física extremadamente difícil de manejar. Por razones que desconocemos esta sustancia está sometida a una fiscalización internacional de menor rango e intensidad que el mencionado 4-MA: no está prohibida; la normativa[2] en este caso nos remite a la exigencia de unos los controles exhaustivos de trazabilidad tanto nacionales como internacionales.
Esto nos lleva a preguntarnos por qué no se actúa de igual forma con la metanfetamina, conocida sustancia psicotrópica que ésta causando estragos con rango de epidemia, generando una adicción física extremadamente difícil de manejar. Por razones que desconocemos esta sustancia está sometida a una fiscalización internacional de menor rango e intensidad que el mencionado 4-MA: no está prohibida; la normativa[2] en este caso nos remite a la exigencia de unos los controles exhaustivos de trazabilidad tanto nacionales como internacionales.
Algo similar ocurre con los precursores de este veneno mortal, la efedrina y la pseudoefedrina, cuyos movimientos deben ser controlados y fiscalizados tanto a nivel nacional como internacional al ser sustancias precursoras de drogas (en este caso de la metanfetamina).
Lo que ocurre es que en la actualidad existen varios medicamentos utilizados para el resfriado común que contienen estos precursores y, cada vez que se ha propuesto a nivel internacional adoptar medidas más exigentes para su control, se han topado con los inconvenientes planteados a través de determinadas empresas farmacéuticas, dado que impediría el acceso a los pacientes a un medicamento lícito que cumple una función.
Parece que no importa que gran parte de esas ventas procedan de compras realizadas por personas vinculadas al tráfico ilícito, que van adquiriendo estos medicamentos sin ningún problema y con la finalidad de extraer el precursor de la metanfetamina. Ante esta situación, no estaría de más que las agencias reguladoras de medicamentos suspendieran la comercialización de estos medicamentos, que no salvan ninguna vida y que son perfectamente sustituibles por otros preparados antigripales que carezcan de los precursores de la metanfetamina.
Para más información recomendamos la visita al documental recientemente se ha podido ver en la 2 de TVE “La epidemia de la metanfetamina“. En INVIFOR siempre nos ha gustado mucho este tema, teniendo a disposición de los profesionales sanitarios interesados en el tema, una actividad información relacionada con todo lo que hay detrás de la fiscalización internacional de estupefacientes, junto con una revisión del lugar en la terapéutica de los opioides.
[1] Convención de las Naciones Unidas de 1988 contra el Tráfico Ilícito de Estupefacientes y Sustancias Psicotrópicas
[2] Convenio sobre Sustancias Psicotrópicas de 1971 de las Naciones Unidas y Real Decreto 2829/1977, de 6 de octubre por el que se regulan las sustancias y preparados medicinales psicotrópicos, así como la fiscalización e inspección de su fabricación, distribución, prescripción y dispensación.
 El Registro constará de 20 datos de los profesionales sanitarios que desarrollan su actividad en España, tanto en el ámbito público como en el privado, y será gestionado por el Ministerio de Sanidad, Servicios Sociales e Igualdad. Se implementará en soporte digital y se facilitará su consulta por medios electrónicos. Los datos que se incorporarán serán los siguientes:
El Registro constará de 20 datos de los profesionales sanitarios que desarrollan su actividad en España, tanto en el ámbito público como en el privado, y será gestionado por el Ministerio de Sanidad, Servicios Sociales e Igualdad. Se implementará en soporte digital y se facilitará su consulta por medios electrónicos. Los datos que se incorporarán serán los siguientes:



Debe estar conectado para enviar un comentario.